转载自:中国食品药品网
中国食品药品网讯 国家药监局发布《药物临床试验机构监督检查办法(试行)》;第九批国家组织药品集中带量采购在上海产生拟中选结果……11月1日—11月7日,医药行业的这些动态值得关注。
行业政策动态
1.国家药监局发布《药物临床试验机构监督检查办法(试行)》,自2024年3月1日起施行。《办法》共六章44条,包括总则、药品检查机构和人员、检查程序、检查有关工作衔接、检查结果的处理、附则,适用于药品监管部门对药物临床试验机构备案及开展以药品注册为目的的药物临床试验活动遵守相关法律法规、执行《药物临床试验质量管理规范》等情况实施检查、处置等。《办法》梳理明确相关部门在试验机构检查方面的职责,强调了试验机构与研究者的主体责任。试验机构和研究者应当切实履行药物临床试验相关责任,授权其他人员承担临床试验有关工作时,应当建立相应管理程序,并采取措施实施质量管理,加强相关信息化建设。研究者应当监督所有授权人员依法依规开展临床试验,执行试验方案、履行工作职责,保护受试者的权益和安全,保障试验数据和结果真实、准确、完整、可靠。
2.国家药监局综合司就《麻醉药品和精神药品实验研究管理规定(征求意见稿)》公开征求意见。与现行《麻醉药品和精神药品实验研究管理规定》相比,征求意见稿框架结构进行了大幅调整,总条目增加超六成,对需要立项的品种范围、申请人和联合研制单位应当具备的条件、研制立项的申报和审批等核心内容进行了修改完善。征求意见截止日期为2023年11月20日。
3.国家药监局药品审评中心(CDE)印发《药品审评中心药物临床试验期间安全信息评估与风险管理工作程序(试行)》。该工作程序指出,临床试验期间,申办者承担药物临床试验安全风险管理主体责任,开展风险监测、识别、评估和控制,并及时向CDE报告可疑且非预期严重不良反应(SUSAR)和其他潜在严重安全性风险信息,定期提交研发期间安全性更新报告(DSUR)。
4.CDE就《中药口服制剂生产过程质量控制研究技术指导原则(征求意见稿)》公开征求意见。征求意见稿提出了中药口服制剂生产过程质量控制的研究策略和关注点,主要阐述了关键物料质量属性和关键过程参数的确立、生产过程质量控制方式的建立、生产过程质量风险的评估和方法验证等内容,旨在为开展相关研究提供指导性意见。征求意见时限为自发布之日起一个月。
5.CDE就《疫苗临床试验的统计学指导原则(征求意见稿)》公开征求意见。征求意见稿针对疫苗临床试验中的关键统计学问题进行阐述,旨在为申办者在疫苗临床试验的设计、实施、分析和评价方面提供指导性建议,主要适用于以支持疫苗注册上市为目的的确证性临床试验。征求意见时限为自发布之日起一个月。
6.CDE网站公示10个仿制药一致性评价任务,涉及注射用氨苄西林钠舒巴坦钠等品种(截至11月7日)。
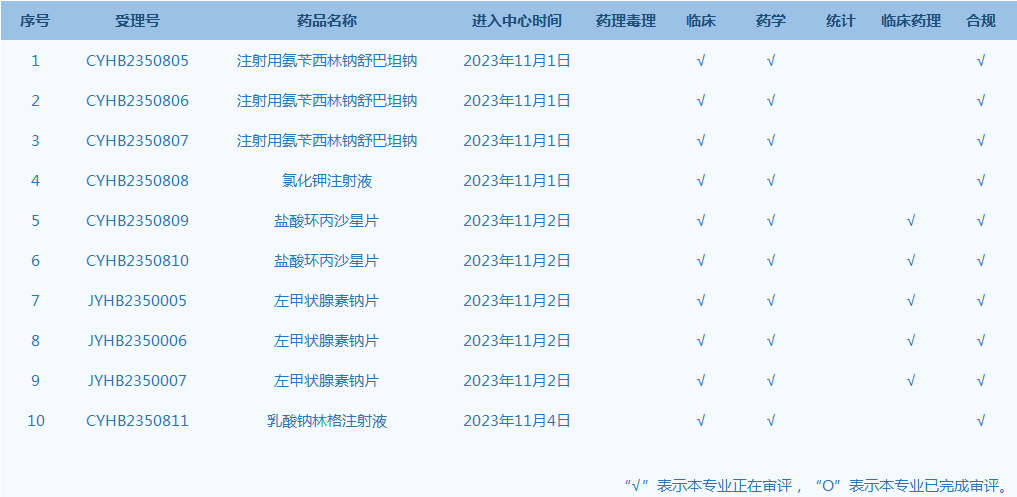
产品研发上市信息
1.国家药监局发布5期药品批准证明文件送达信息,共包括154个受理号,涉及拜耳医药保健有限公司等企业(截至11月7日)。
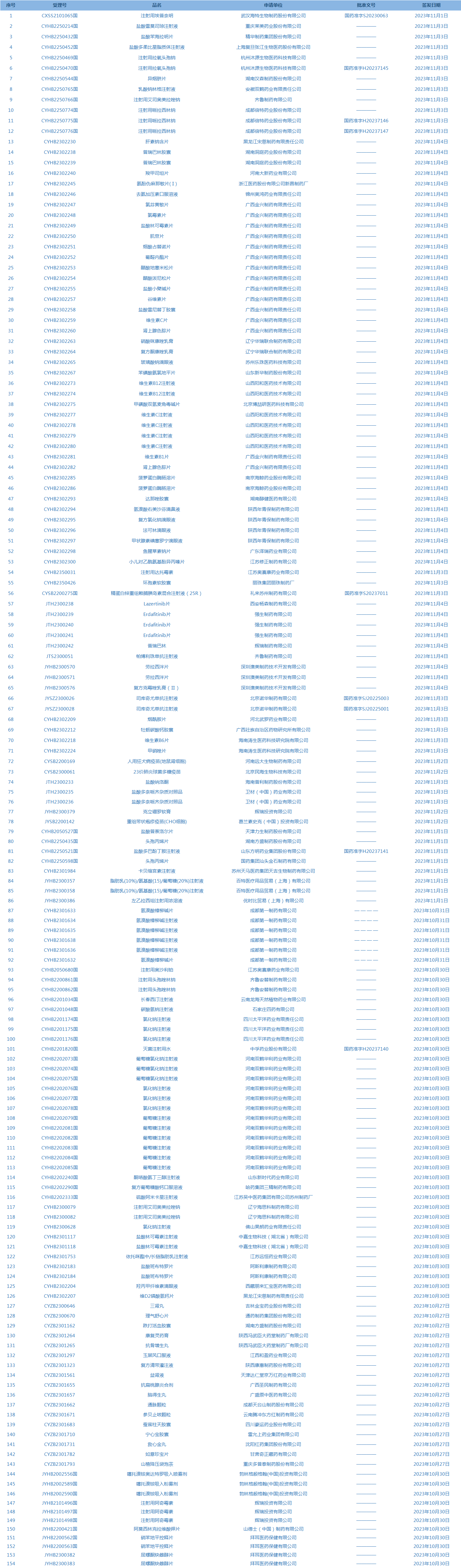
2.CDE承办受理61个新药上市申请,包括AZD0901等药品(截至11月7日)。
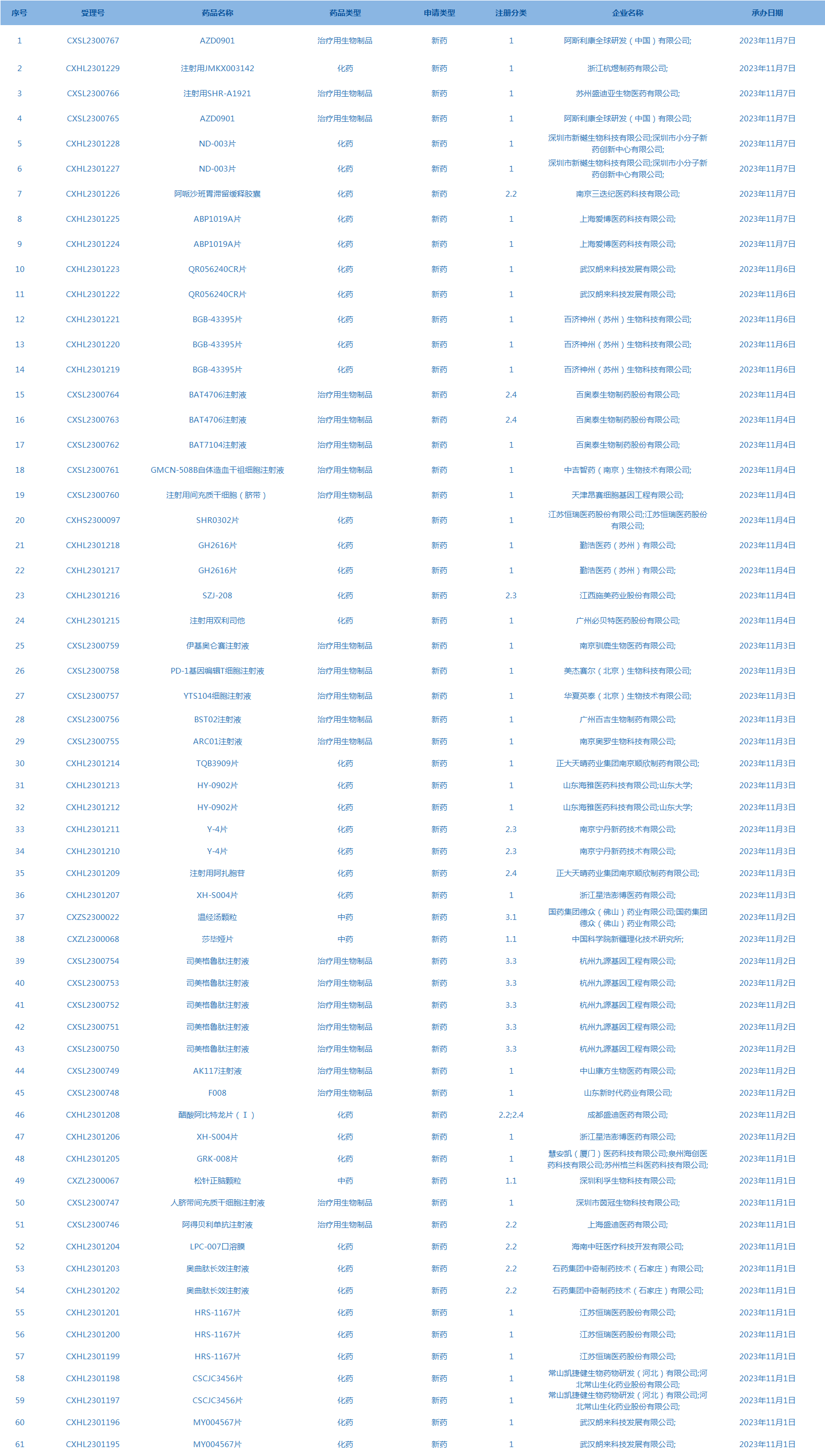
3.康弘药业发布公告称,收到美国食品药品管理局(FDA)的通知,同意KH629开展新药临床试验。
4.三叶草生物宣布,公司已完成向巴西国家卫生监督管理局 (ANVISA) 基于其季节性流感疫苗的上市申报。
5.华海药业发布公告称,其下属子公司华奥泰生物收到美国FDA批准注射用HB0052用于晚期实体瘤的新药临床试验(IND)申请。
医药企业观察
1.普米斯生物宣布与德国BioNTech公司达成一项许可和合作协议。根据协议条款,BioNTech公司将获得普米斯生物自主研发的抗PD-L1/VEGF双特异性抗体PM8002在全球(大中华区除外)的开发、生产和商业化权利,普米斯生物将相应地获得5500万美元的首付款,以及超10亿美元的开发、注册和商业里程碑付款以及分级销售提成。
2.基石药业宣布与三生制药附属公司沈阳三生制药就抗PD-1单抗nofazinlimab签订在中国大陆地区的许可协议。依据许可协议条款,基石药业将从此次交易中获得6000万元人民币的首付款、上限达近亿元人民币的研发及注册里程碑付款,以及商业化阶段的销售里程碑付款和梯度销售分成。三生制药将获得nofazinlimab在中国大陆地区开发、注册、生产和商业化的独家授权。基石药业将保留nofazinlimab在中国大陆以外地区的权利并将积极寻求合作伙伴。
3.翰宇药业发布公告称,收到美国某大型制药公司的采购订单,其将向公司合计采购累计金额1408.32万美元(含税约合人民币1.03亿元)的利拉鲁肽注射液(仿制药)。
4.赛生药业发布公告称,公司已与美纳里尼集团旗下BerlinChemie AG订立许可及合作协议,授权集团根据此前美纳里尼与Radius Health, Inc.的总许可协议于中国独家开发及商业化Orserdu (Elacestrant)。根据许可协议,赛生药业将利用其开发能力开展临床试验,并利用其在销售、营销及监管方面的专业知识在中国获得批准后分销Orserdu。赛生药业将以现金向美纳里尼支付一笔预付款,并在达到各监管及销售里程碑时支付额外款项。美纳里尼亦将根据Orserdu在中国的净销售额收取分级特许权使用费。
药品集中采购
1.第九批国家组织药品集中带量采购在上海产生拟中选结果。此次集采有41种药品采购成功,拟中选药品平均降价58%,预计每年可节约药费182亿元。
2.安徽省医药联合采购办公室就《安徽省中成药带量联动工作实施方案(征求意见稿)》公开征求意见。征求意见稿显示,黄山市医疗保障局负责2023年安徽省中成药带量联动项目。本次带量联动涉及14个品种28个药品,采用带量询价的方式开展,询价价格参考该产品在湖北联盟第一批、广东联盟、山东省集采产品的最低中选价格及安徽省相关药品挂网采购价。
Copyright © 2011-2012 350浦京首页集团 All Rights Reserved. 粤ICP备2022155250号-1
电
话:0755-82497618 传 真:0755-82497861